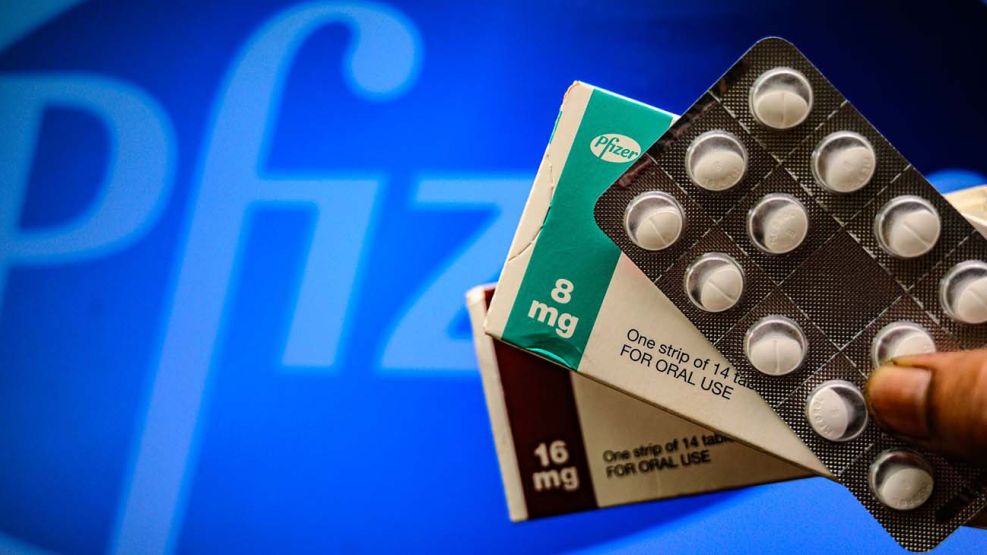
La farmacéutica Pfizer Inc. firmó un acuerdo con un grupo respaldado por las Naciones Unidas (ONU) para permitir que otras compañías fabriquen su píldora experimental contra el Covid-19.
Según informó la compañía este martes 16 de noviembre, se trata de una medida que podría hacer que el tratamiento esté disponible para más de la mitad de la población mundial.
Mediante un comunicado, Pfizer detalló que otorgaría una licencia para la píldora antiviral al Fondo de Patentes de Medicamentos con sede en Ginebra, Suiza.
Esto posibilitaría a las compañías de medicamentos genéricos producirla para su uso en 95 países, lo que representa aproximadamente el 53% de la población mundial.
Pfizer anunció que su pastilla contra el Covid-19 reduce en un 89% el riesgo de muerte
Días atrás, Pfizer había informado que su pastilla para el Covid-19, bautizada Paxlovid, redujo en un 89% las hospitalizaciones y muertes en pacientes de alto riesgo, un resultado que tiene el potencial de cambiar la forma en que se trata la enfermedad causada por el coronavirus y alterar el curso de la pandemia.
La farmacéutica dijo que dejó de aceptar nuevos pacientes en un ensayo clínico del tratamiento “debido a la abrumadora eficacia” del fármaco, y que planeaba presentar los resultados a las autoridades reguladoras estadounidenses para obtener una autorización de emergencia lo antes posible.
Al día de hoy ya hay dos candidatos prometedores para tratar a los pacientes en las primeras fases de la enfermedad. El mes pasado, Merck & Co. y su socio Ridgeback Biotherapeutics LP presentaron su píldora experimental a los reguladores después de que un estudio demostrara que reducía a la mitad el riesgo de enfermar gravemente o morir en pacientes con covid-19 leve a moderado.
Qué se sabe sobre la pastilla anticovid de Pfizer, que reduce hospitalizaciones y muertes un 89%
Cómo es el accionar de Paxlovid
En el ensayo realizado por Pfizer en 1.219 adultos no vacunados, cinco días de tratamiento con su fármaco redujeron drásticamente la tasa de hospitalización cuando se empezó a tomar dentro de los tres o cinco días posteriores al inicio de los síntomas, informó la empresa.
En general, solo el 0,8% de las personas que comenzaron el tratamiento dentro de los tres días posteriores a la aparición de los síntomas terminaron en el hospital y nadie murió, mientras que el 7% de las personas que recibieron un placebo en esa franja de tiempo posteriormente fueron hospitalizadas o murieron.
Desarrollada internamente por investigadores de Pfizer en EE.UU. y el Reino Unido, el fármaco Paxlovid se une a una enzima llamada proteasa para evitar que el virus se replique. Algunos medicamentos para el VIH funcionan de manera similar.
Pfizer anunció que su pastilla contra el Covid-19 reduce en un 89% el riesgo de muerte
Según detalló la compañía, se desarrolló a partir de un antiguo fármaco antiviral experimental que Pfizer había desarrollado tras la epidemia original de SARS, un coronavirus primo del covid-19 que mató a unas 800 personas a partir de fines de 2002.
Ese fármaco se administraba por vía intravenosa, pero en julio de 2020 los investigadores de Pfizer modificaron la molécula original y crearon un nuevo compuesto que resultó ser muy potente contra el covid-19 y otros coronavirus en el tubo de ensayo, y que podía utilizarse en forma de píldora.
ag / ds