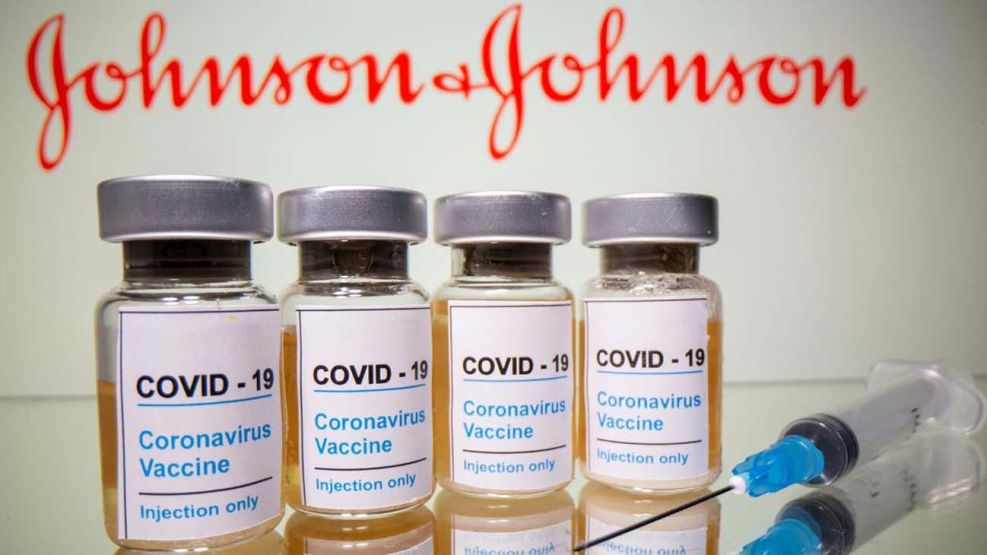
El uso de la vacuna contra el covid-19 de Johnson & Johnson será restringido a adultos estadounidenses a quienes otras vacunas no les resultan apropiadas, después de una investigación relacionada con el un trastorno de coagulación inusual y potencialmente mortal que ocurre en algunos receptores.
La Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) limitó el uso de la vacuna a personas mayores de 18 años para quienes otras vacunas no son accesibles o clínicamente apropiadas, y aquellos que de otro modo no se inmunizarían contra el virus. La monodosis de J&J se ha destacado por su conveniencia en comparación con las vacunas de dos dosis, especialmente en áreas remotas y en poblaciones como la de las personas sin hogar, a quienes puede resultarles difícil administrar inmunizaciones repetidas.

La aceptación de la vacuna J&J ha palidecido en comparación con las fabricadas por Pfizer Inc. y Moderna Inc., que requieren dos dosis para un régimen completo. Hasta ahora se han administrado cientos de millones de sus vacunas de ARN mensajero. Aunque se han administrado unos 18,7 millones de dosis de la vacuna de J&J a adultos estadounidenses, según los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés), se han entregado casi 31 millones de dosis a los sitios de vacunas, lo que sugiere un excedente de vacunas sin usar.
Descubren más de 1.000 efectos secundarios de la vacuna de Pfizer
La agencia decidió limitar el uso autorizado de la vacuna de J&J después de realizar una investigación y un análisis de los casos informados de coágulos de sangre en combinación con niveles bajos de plaquetas en la sangre, conocido como síndrome de trombosis con trombocitopenia o TTS, que ocurrieron una o dos semanas después de la administración del vacuna
Los hallazgos de ese análisis “justifican la limitación del uso autorizado de la vacuna”, dijo la FDA en el comunicado, lo que sugiere que los beneficios potenciales solo superan los riesgos para aquellos para quienes otras vacunas no son accesibles.