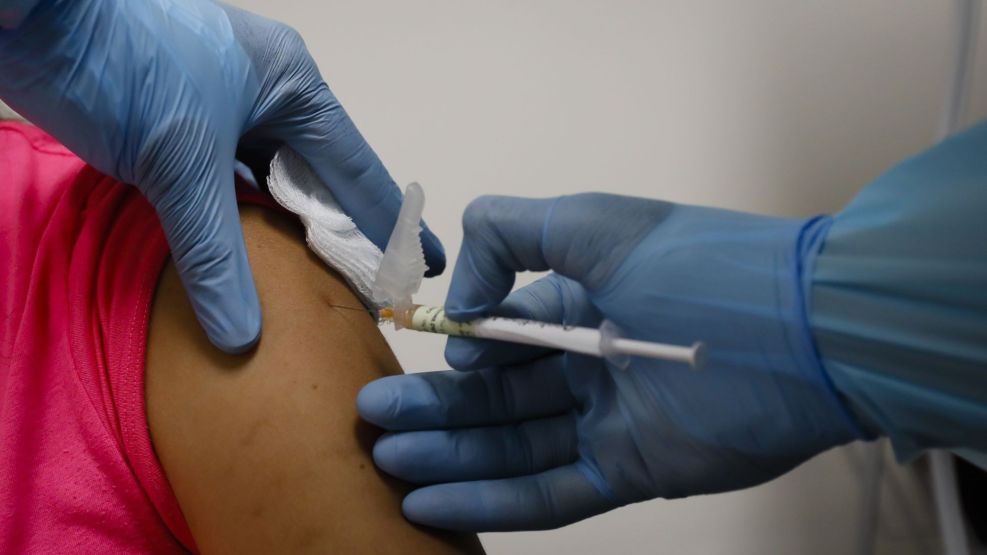
La vacuna experimental de Pfizer Inc. para una infección pulmonar potencialmente peligrosa llamada virus sincicial respiratorio, alcanzó su objetivo principal de prevenir los síntomas en un gran ensayo de 37.000 adultos mayores.
En base a los resultados, la compañía planea solicitar este otoño la aprobación de Estados Unidos, según un comunicado, lo que convierte al producto en un posible candidato temprano a lo que podría ser un gran mercado nuevo de vacunas contra enfermedades respiratorias.
Pfizer anticipa que podría obtener una revisión prioritaria de la vacuna, lo que acortaría su camino hacia el mercado, dijo William Gruber, director de investigación y desarrollo de vacunas clínicas de la empresa, en una entrevista.
El fabricante de medicamentos está compitiendo contra rivales como GSK Plc, Johnson & Johnson y Moderna Inc. para probar y comercializar vacunas contra el virus, y recibió el estado de terapia innovadora para su candidata en marzo. La enfermedad es peligrosa para las personas mayores y aquellas con sistemas inmunitarios débiles, dando cuenta de unas 177.000 hospitalizaciones y 14.000 muertes entre ancianos estadounidenses cada año, según un estudio de 2005.
La farmacéutica británica GSK dijo en junio que su vacuna candidata fue eficaz para prevenir el VSR en un ensayo de aproximadamente 25.000 adultos de 60 años o más. GSK aclaró entonces que era el primer ensayo exitoso en etapa final de una vacuna para el VSR en adultos mayores, y que la compañía solicitaría la autorización en la segunda mitad del año. No publicó resultados detallados en ese momento.
Disminución de síntomas
El ensayo de Pfizer tenía como objetivo mostrar si su vacuna experimental puede prevenir los síntomas del VSR en el sistema respiratorio inferior de los adultos mayores que podrían convertirse en casos que requieran hospitalización. Los síntomas medidos en el ensayo incluyeron tos, sibilancias, aumento de la producción de flema, dificultad para respirar y respiración rápida, dijo Gruber. Cuando los pacientes llegaban con estos síntomas, se les hacían pruebas para confirmar que el VSR era la causa.
Entre los adultos de 60 años o más, la vacuna experimental de Pfizer tuvo una eficacia del 66,7% en la prevención de casos de VSR con dos o más síntomas respiratorios en las vías respiratorias inferiores, y una eficacia del 85,7% en la prevención de casos con tres o más de esos síntomas, dijo la compañía.
No aparecieron problemas significativos de seguridad en el ensayo, dijo la compañía.
La compañía no dio a conocer todos los detalles de los resultados, que planea presentar en una próxima conferencia médica y enviar para su publicación en una revista científica. Pero Gruber dijo que ambos resultados parecían cumplir con los criterios mínimos de eficacia de la la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) para las vacunas contra el VSR. El ensayo no se ha extendido lo suficiente como para demostrar si la vacuna realmente previene las hospitalizaciones, dijo.
Una sola dosis
La vacuna consiste en una dosis única que contiene formas estabilizadas de una proteína crucial que el virus usa para unirse e ingresar a las células humanas. Al igual que la influenza, otro virus pulmonar común, el VSR es estacional. Pfizer continúa con su ensayo en adultos para ver si una vacuna brinda protección durante más de una temporada de VSR, dijo Gruber.
Pfizer dijo que planeaba solicitar la aprobación en otros países poco después de su presentación ante la FDA.
La enfermedad también es común en bebés, y Pfizer está realizando un ensayo para probar la vacuna en mujeres embarazadas. La esperanza es que las madres inoculadas transmitan anticuerpos a sus bebés, protegiéndolos del VSR en sus primeros meses de vida.
LM / MCP