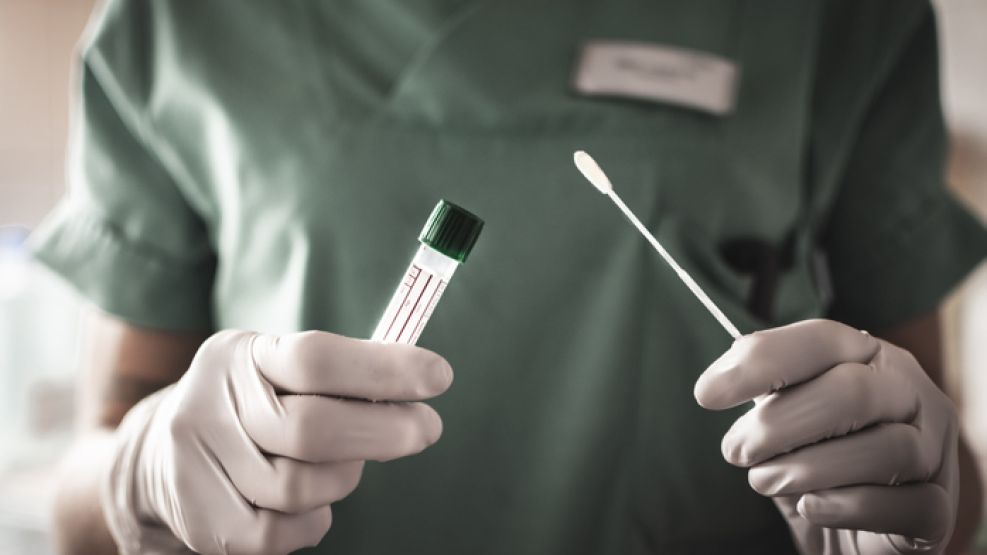
La prueba, conocida como CareStart, forma parte de un grupo de nuevas pruebas de antígenos que detectan el nuevo coronavirus mediante la búsqueda de proteínas en su superficie.
Debido a que la detección de antígenos puede proporcionar resultados rápidos en los consultorios médicos, las clínicas de atención de urgencia y los hospitales, podrían tener un papel clave en la expansión del acceso a las pruebas y en el suministro de información oportuna a los pacientes y proveedores. Pero el uso de estas pruebas ha sido limitado. Inicialmente, el Gobierno compró muchas pruebas para su uso en hogares de ancianos, y se están realizando esfuerzos para extender más el uso de las pruebas en los estados y en entornos como escuelas.
“Para reabrir la sociedad, necesitaremos realizar estas pruebas rápidas”, dijo Reeve Benaron, fundador de Intrivo Diagnostics, la división de Access Bio en EE.UU.
CareStart es un producto autónomo de un solo uso que funciona con tecnología de flujo lateral, similar a las pruebas de embarazo caseras. La prueba incluye un hisopo, un vial de solución de extracción y un casete del tamaño de una pequeña unidad flash. Aparece una línea visible en el casete si la prueba es positiva, y no se requiere capacitación especial para administrarla, dijo Crystal Nguyen, jefa de investigación y desarrollo de Intrivo.
El costo será de menos de US$20 por prueba, aunque el precio exacto depende del volumen comprado, dijo Benaron. Eso la hace competitiva con una prueba de antígeno de US$20 vendida por Becton Dickinson & Co. que requiere equipo adicional para producir un resultado.
Otra prueba de antígeno autónoma de Laboratorios Abbott que esté verano recibió la autorización para su venta en EE.UU. tiene un precio de solo US$ 5. El Gobierno de EE.UU. compró 150 millones de pruebas de antígeno BinaxNOW de Abbott a fines de agosto, que está distribuyendo a los estados, potencialmente para su uso en lugares como escuelas, así como también en centros para el cuidado de ancianos, universidades históricamente negras y tribus de americanos nativos.
Cuándo sale a la venta el test rápido
La compañía planea comenzar a vender las pruebas en noviembre y tiene el objetivo de producir alrededor de 10 millones mensuales para fines de noviembre, y de 60 millones a 80 millones mensuales a mediados de febrero, cuando se espera que abra una nueva fábrica, según Benaron.
La gran mayoría de las pruebas producidas se venderán en Estados Unidos, a centros de atención médica, al Gobierno y al sector privado, dijo.
Benaron señaló que ha observado un interés particular en la prueba de antígeno por parte de los líderes de las compañías Fortune 500. “Se ven obligados a tomar decisiones médicas. Ya no son solo directores ejecutivos”, dijo. “Son aguas sin precedentes e inexploradas”.
Las pruebas de detección de antígenos, si bien son rápidas, también son menos precisas que las pruebas de diagnóstico de PCR estándar, y las preocupaciones giran principalmente en torno a las pruebas que no detectan a personas infectadas.
Qué pasa con los falsos positivos
Las preocupaciones sobre el fenómeno opuesto, o los falsos positivos, llevaron a Nevada a decirle a los hogares de ancianos este mes que dejen de usar pruebas de antígenos para evaluar a los residentes y trabajadores. Sin embargo, los fabricantes y funcionarios del Gobierno dicen que algunos falsos positivos son inevitables con cualquier prueba.
CareStart es 88,4% sensible, una medida de la frecuencia con la que detecta correctamente las infecciones, y 100% específica, la tasa de pruebas negativas correctas, dijo Nguyen.
“No está destinada a reemplazar a la PCR” y, de hecho, un resultado positivo se confirmará con una prueba de PCR, dijo Benaron.