Pfizer Inc. y su socio BioNTech SE solicitaron una aprobación regulatoria para su vacuna contra el covid-19 en la Unión Europea, con lo que la vacuna podría recibir una autorización antes de fin de año.
La Agencia Europea de Medicamentos (EMA, por sus siglas en inglés) informó el martes que podría entregar su resolución dentro de unas semanas y está prevista para el 29 de diciembre, a más tardar, una reunión sobre la evaluación. La solicitud formal enviada el lunes pone término a un proceso de revisión continua que comenzó el 6 de octubre y permitió al regulador europeo de medicamentos evaluar los datos sobre la vacuna a medida que iban surgiendo.
Gobiernos de todo el mundo están ansiosos por comenzar a vacunar a sus poblaciones para frenar la pandemia. El lunes, la farmacéutica rival Moderna Inc. solicitó autorización en Estados Unidos y Europa. El Reino Unido invocó una norma especial para permitir que su regulador se salte a su homólogo de la UE y pueda ser el primero en aprobar el producto de Pfizer-BioNTech. EE.UU. no se encuentra mucho más atrás, ya que un panel de la Administración de Alimentos y Medicamentos (FDA) se reunirá el 10 de diciembre para discutir sobre la vacuna.
BioNTech puede comenzar a enviar las primeras dosis “en cuestión de horas” después de la aprobación regulatoria, dijo el director financiero de la farmacéutica, Sierk Poetting, en una conferencia de prensa.
En noviembre, un estudio de casi 44.000 personas mostró que la vacuna previno el 95% de los casos sintomáticos de coronavirus.
Si la EMA concluye que los beneficios de la vacuna de Pfizer-BioNTech superan sus riesgos, recomendará otorgar una autorización condicional que permita la implementación en Europa antes de fin de año, dijeron las compañías en un comunicado. La agencia dijo que trabajaría “durante el período de Navidad” en la evaluación.
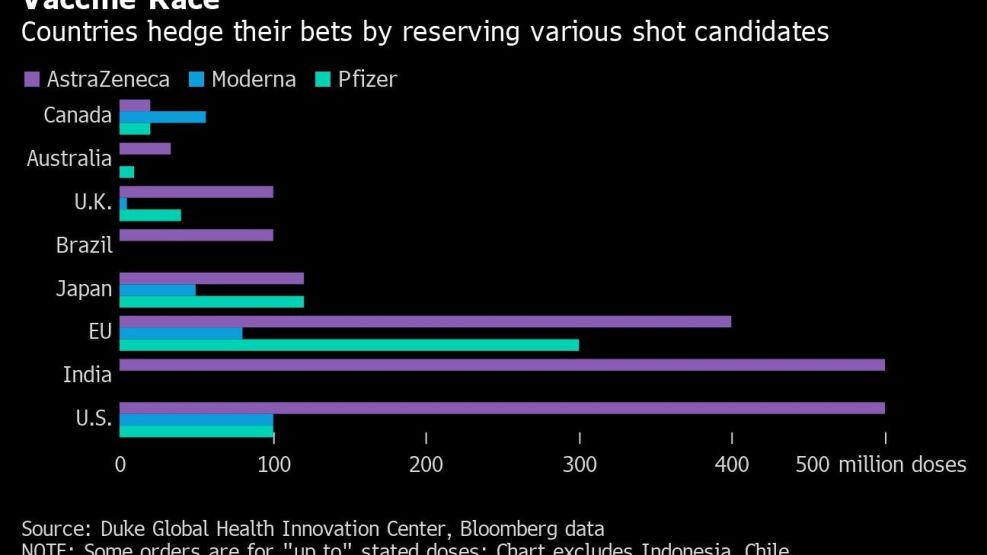
Pfizer y BioNTech también iniciaron presentaciones regulatorias en otros países, como Australia, Canadá y Japón, señalaron. Los socios han firmado acuerdos para suministrar cientos de millones de dosis de la vacuna, incluido un acuerdo con la UE para la entrega de 200 millones de dosis, con una opción para 100 millones adicionales.
Una autorización condicional se emite cuando las autoridades europeas desean administrar rápidamente un medicamento a pacientes sin esperar un compendio de datos tan completo como se requeriría normalmente para una autorización estándar. Es válido por un año y renovable y, en última instancia, podría convertirse en una aprobación estándar.