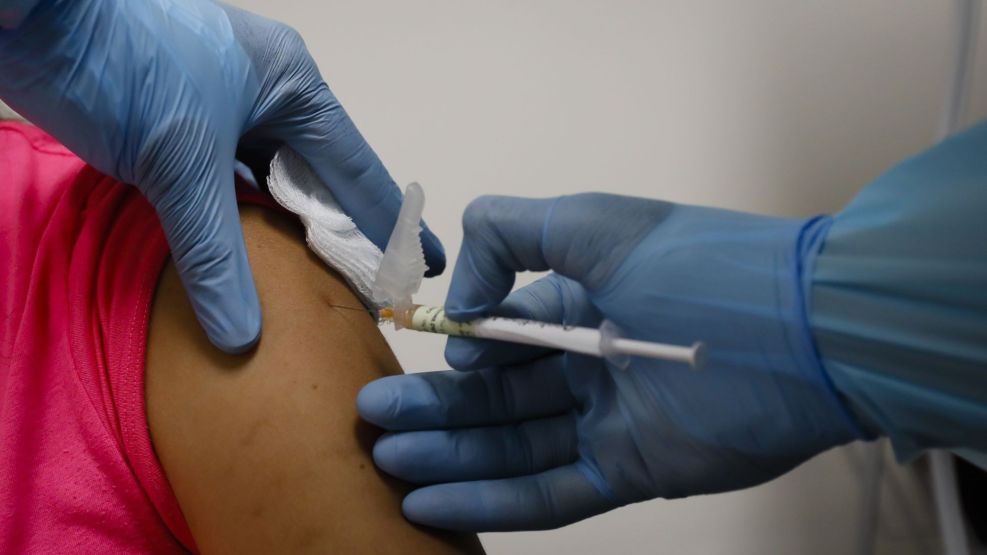
Una solicitud de aprobación de emergencia de la vacuna contra el covid-19 desarrollada por la alianza Pfizer/BioNTech podría ser presentada este viernes 20 de noviembre en Estados Unidos.
"El socio de Pfizer, BioNTech, anunció que tiene la intención de presentar mañana (viernes) una solicitud de emergencia para la aprobación" de su vacuna ante la agencia reguladora de medicamentos de Estados Unidos (FDA), dijo el secretario de Salud estadounidense, Alex Azar.
Agregó que el gobierno estadounidense "espera" que Moderna, una compañía estadounidense que también compite para desarrollar y distribuir una vacuna contra el covid-19, "presente pronto" su solicitud de aprobación.
Más temprano, el cofundador de BioNTech, Ugur Sahin, dijo en una entrevista: "Los documentos serán finalizados hoy (jueves) y mañana y presentados a la FDA". Y el director general de Pfizer había dicho el martes que muy pronto se presentaría una solicitud de autorización en Estados Unidos.
Coronavirus: Pfizer anuncia que su vacuna elevó su efectividad al 95%
El gigante farmacéutico estadounidense Pfizer y BioNTech, una pequeña empresa alemana de biotecnología, anunciaron el miércoles que su vacuna era efectiva en un 95% para la prevención del covid-19, según los resultados completos de su ensayo clínico a gran escala.
Una autorización de emergencia es una autorización temporal o condicional concedida para responder a una situación de urgencia como una pandemia. Puede ser revocada o modificada si posteriormente surgen nuevos datos de eficacia o seguridad de la sustancia.
El proyecto de los laboratorios Pfizer/BioNTech es, con el del estadounidense Moderna, el más avanzado en los ensayos clínicos a gran escala, en ambos casos con una eficacia comparable del 95%.
Centenares de millones de dosis ya fueron reservadas en el mundo, pero varios gobiernos anunciaron que las inyecciones serán de antemano destinadas al personal médico y a los más vulnerables. El resto de la población deberá esperar varios meses.
Son marido y mujer, millonarios y responsables de una de las vacunas contra el coronavirus
Protección "al menos durante un año"
Si "todos los actores, entre ellos gobiernos, empresas farmacéuticas y la cadena logística hacen un buen trabajo, podemos vacunar entre 60% al 70% de la población de aquí al invierno de 2021", dijo esta semana Ugur Sahin. "Si lo logramos, podemos tener un invierno normal, sin nuevo 'confinamiento'", agregó el científico, cofundador de BioNTech, con sede en Maguncia (Alemania).
Pfizer/BioNTech ya firmó varios contratos, especialmente con la UE y Estados Unidos, y negocia actualmente "con 30 países" más. Los laboratorios hablan con "varias organizaciones", entre ellas Naciones Unidas, para que "la vacuna esté disponible para todos en el mundo" y reducir su costo para que pueda ser accesible en los países pobres.
Sahin, de 55 años, y su mujer Özlem Türeci, directora médica y cofundadora de la empresa, se harán "por supuesto" vacunar cuando sea posible. Sahin se muestra "muy confiado" en la seguridad de la vacuna.
El equipo detrás de una de las vacunas contra el coronavirus
Hasta ahora "ningún efecto secundario grave" ha sido constatado en los ensayos a gran escala. "De manera razonable, diría que la vacuna protegerá al menos un año, e incluso más", indicó Sahin.
Otro problema es la distribución de este producto, que requiere ser conservado a muy baja temperatura, -70 grados Celsius, y no más de cinco días con una temperatura de refrigerador. Desconocidos del gran público hasta hace poco, los fundadores de BioNTech llamaron la atención por su recorrido de hijos de inmigrantes turcos, formados en Alemania.
La pareja creó la empresa en 2008 con el objetivo de de desarrollar una nueva generación de terapias individuales para enfermos de cáncer.
ds