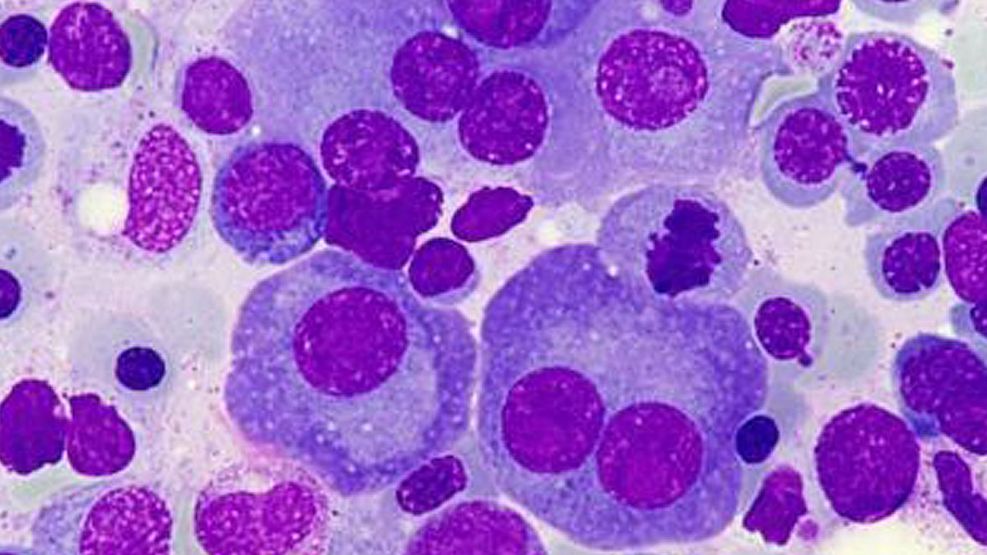
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) aprobó un nuevo tratamiento para el mieloma múltiple en estado avanzado, una enfermedad oncológica de la sangre que, aunque presenta avances terapéuticos en las últimas décadas, continúa siendo incurable.
Tuberculosis: la pieza que falta para frenar la mayor amenaza infecciosa del mundo
El medicamento, denominado talquetamab, está indicado para pacientes adultos con mieloma múltiple en recaída o refractario que ya hayan sido sometidos a al menos tres líneas de tratamiento previas y cuya enfermedad haya progresado. La aprobación representa una nueva alternativa para un grupo de pacientes con opciones terapéuticas limitadas.
Qué es el mieloma múltiple y por qué es difícil de tratar
El mieloma múltiple es un tipo de cáncer hematológico que afecta a las células plasmáticas, responsables de producir anticuerpos en la médula ósea. En esta enfermedad, las células anormales se multiplican sin control, generan anticuerpos defectuosos y afectan la producción normal de células sanguíneas.
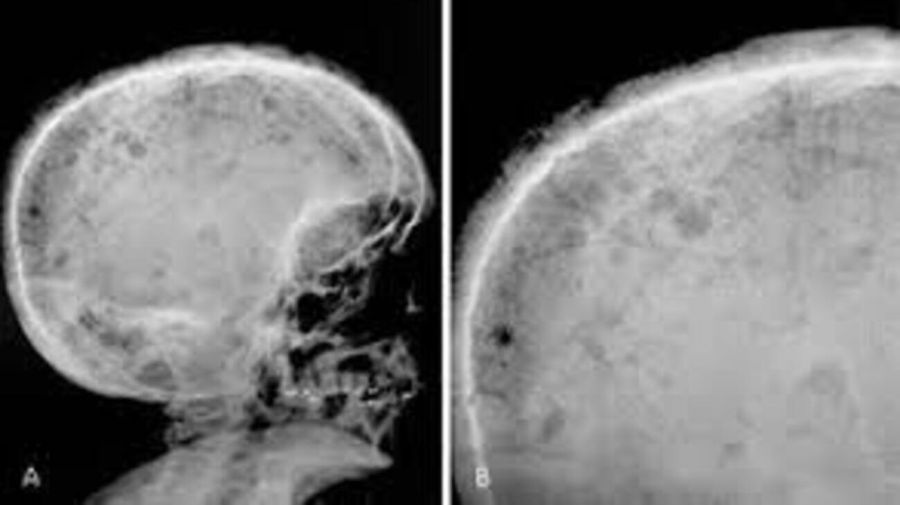
Esto puede derivar en complicaciones severas como anemia, insuficiencia renal, infecciones recurrentes, fracturas óseas y niveles elevados de calcio en sangre.
En Argentina, se estiman alrededor de 1.300 nuevos casos por año, con mayor incidencia en personas entre los 50 y 70 años. A pesar de los avances médicos, la enfermedad presenta una alta tasa de recaída: la mayoría de los pacientes deja de responder a los tratamientos con el tiempo, y la probabilidad de sobrevida tras una tercera línea terapéutica se reduce significativamente.
Cómo funciona el nuevo tratamiento aprobado
Talquetamab es un anticuerpo biespecífico con un mecanismo innovador: actúa sobre dos blancos terapéuticos simultáneamente. Por un lado, se une al receptor CD3 presente en las células T del sistema inmunológico; por otro, al receptor GPRC5D, que se expresa en las células tumorales.
Este doble anclaje permite redirigir las células T del propio paciente hacia las células cancerosas, activando una respuesta inmune que ataca directamente al tumor.
Según los resultados del estudio clínico MonumenTAL-1, en el que participaron más de 300 pacientes, el tratamiento logró tasas de respuesta global del 74% en pacientes sin terapias previas de este tipo y del 67% en aquellos que ya habían sido tratados con terapias inmunológicas similares.
Además, se observó una duración media de la respuesta de hasta 17,5 meses y una tasa de supervivencia global del 67,1% a los dos años.
Modo de administración y perfil de seguridad
El tratamiento se administra mediante inyección subcutánea, con una fase inicial de escalado progresivo y luego una aplicación quincenal. Esta modalidad permite, en muchos casos, su uso ambulatorio bajo control médico.
Entre los efectos adversos más frecuentes se registraron alteraciones del gusto, sequedad bucal, pérdida de peso e infecciones, en su mayoría de intensidad leve a moderada y de carácter transitorio.
Una nueva esperanza para pacientes sin alternativas
Especialistas en hematología destacaron la relevancia de esta aprobación. La médica hematóloga María Eugenia Funes señaló que la incorporación de talquetamab amplía el abanico terapéutico para pacientes que ya no responden a tratamientos convencionales.
Alerta en Santa Fe: investigan la muerte de una mujer como posible primer caso de dengue de 2026
En la misma línea, el hematólogo Cristian Seehaus afirmó que en la práctica clínica es habitual encontrar pacientes que agotaron las opciones disponibles, por lo que la llegada de este fármaco representa una nueva oportunidad de tratamiento.
Desde el laboratorio desarrollador también remarcaron el impacto del avance, al considerar que esta terapia ofrece una posibilidad concreta para mejorar la sobrevida en una población históricamente desatendida.
LV/ff