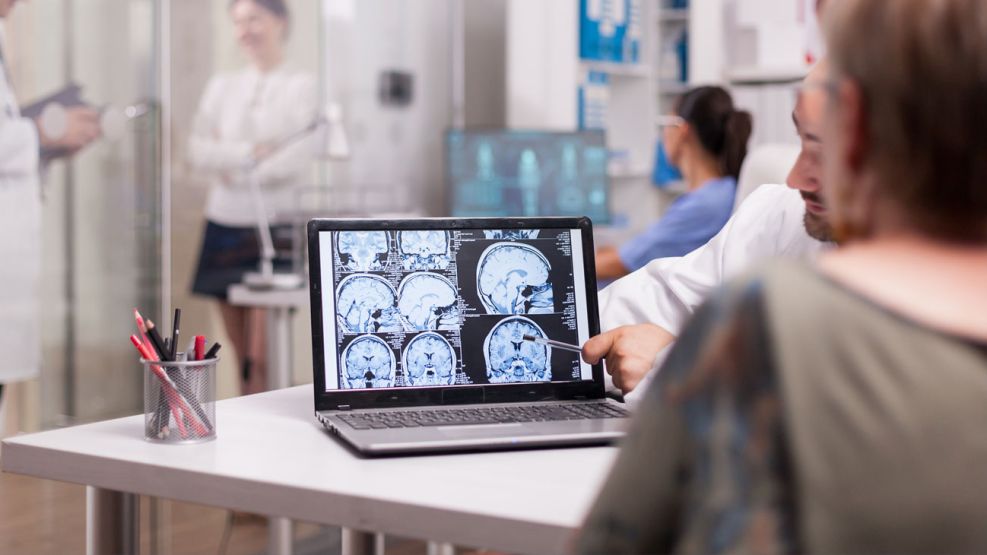
El equipo de científicos del Centro de Cáncer de la Universidad de Florida desarrolló una vacuna personalizada que utilizó el propio ácido ribonucleico (ARNm) de los pacientes para combatir el glioblastoma multiforme. Esta patología afectó a más de 100.000 personas en Estados Unidos y se consideró una de las formas más letales de cáncer cerebral por su resistencia a los tratamientos convencionales. El ensayo clínico Fase 1, cuyos resultados difundió la revista Cell, demostró que la terapia logró activar una respuesta inmunitaria inmediata.

La publicación especializada Cell detalló que el procedimiento consistió en extraer material genético del tumor de cada paciente para fabricar una vacuna específica. A diferencia de otras inmunoterapias que tardaron semanas en estar listas, este sistema permitió la administración del fármaco en un plazo menor a un día. Los cuatro adultos que participaron del estudio mostraron una actividad defensiva superior a la registrada en tratamientos previos, extendiendo su sobrevida más allá de las proyecciones iniciales de los médicos.
"Ver que el sistema inmunitario responde con tanta fuerza y tan rápido fue algo que no esperábamos", expresó el doctor Duane Mitchell, autor principal de la investigación. El método aplicó una tecnología de nanopartículas que envolvió el código genético del tumor, permitiendo que las células blancas identificaran la amenaza de forma directa. Este avance buscó superar la barrera hematoencefálica, que usualmente impidió que los medicamentos llegaran al tejido cerebral afectado.
Salud pública en alerta: crecen los brotes y cae la cobertura de vacunación infantil en Argentina
Cómo funciona la vacuna de ARNm contra el cáncer cerebral
El proceso comenzó con la toma de una muestra del tumor mediante cirugía. Los técnicos aislaron el ARN mensajero y lo replicaron para luego insertarlo en partículas lipídicas. Al inyectar esta mezcla en el torrente sanguíneo, el cuerpo del paciente interpretó que las células cancerosas eran un virus invasor. El sistema inmunitario generó una respuesta inflamatoria masiva que atacó exclusivamente a las células malignas, preservando el tejido sano circundante.
Los datos del ensayo arrojaron que la respuesta se activó en apenas unas horas. En los modelos animales previos, los investigadores observaron que la vacuna reprogramó el microambiente tumoral. Los resultados en humanos confirmaron que los niveles de citocinas subieron drásticamente tras la primera dosis.

Vacuna antigripal 2026: quiénes deben vacunarse gratis y qué se sabe de la variante H3N2
Qué impacto tiene este avance para el futuro de la oncología
La implementación de vacunas personalizadas marcó un cambio de paradigma en el abordaje de enfermedades incurables. Al tratar cada caso como una variante genética única, la medicina de precisión aumentó las chances de éxito en cuadros donde la quimioterapia falló. El glioblastoma tuvo históricamente una tasa de supervivencia baja, con una media de 15 meses tras el diagnóstico inicial. Con este nuevo esquema, los pacientes alcanzaron meses adicionales de vida con una calidad funcional superior.

"Lo que logramos fue convertir al propio cuerpo en la fábrica de su medicina", puntualizó Elias Sayour, oncólogo pediátrico que participó en el diseño del protocolo. El estudio se expandió a una Fase 2 que incluirá a un grupo más numeroso de voluntarios, incluyendo niños, para verificar la seguridad a largo plazo. Los científicos proyectaron que esta plataforma de ARNm podría adaptarse para otros tipos de tumores sólidos en el futuro cercano.
API